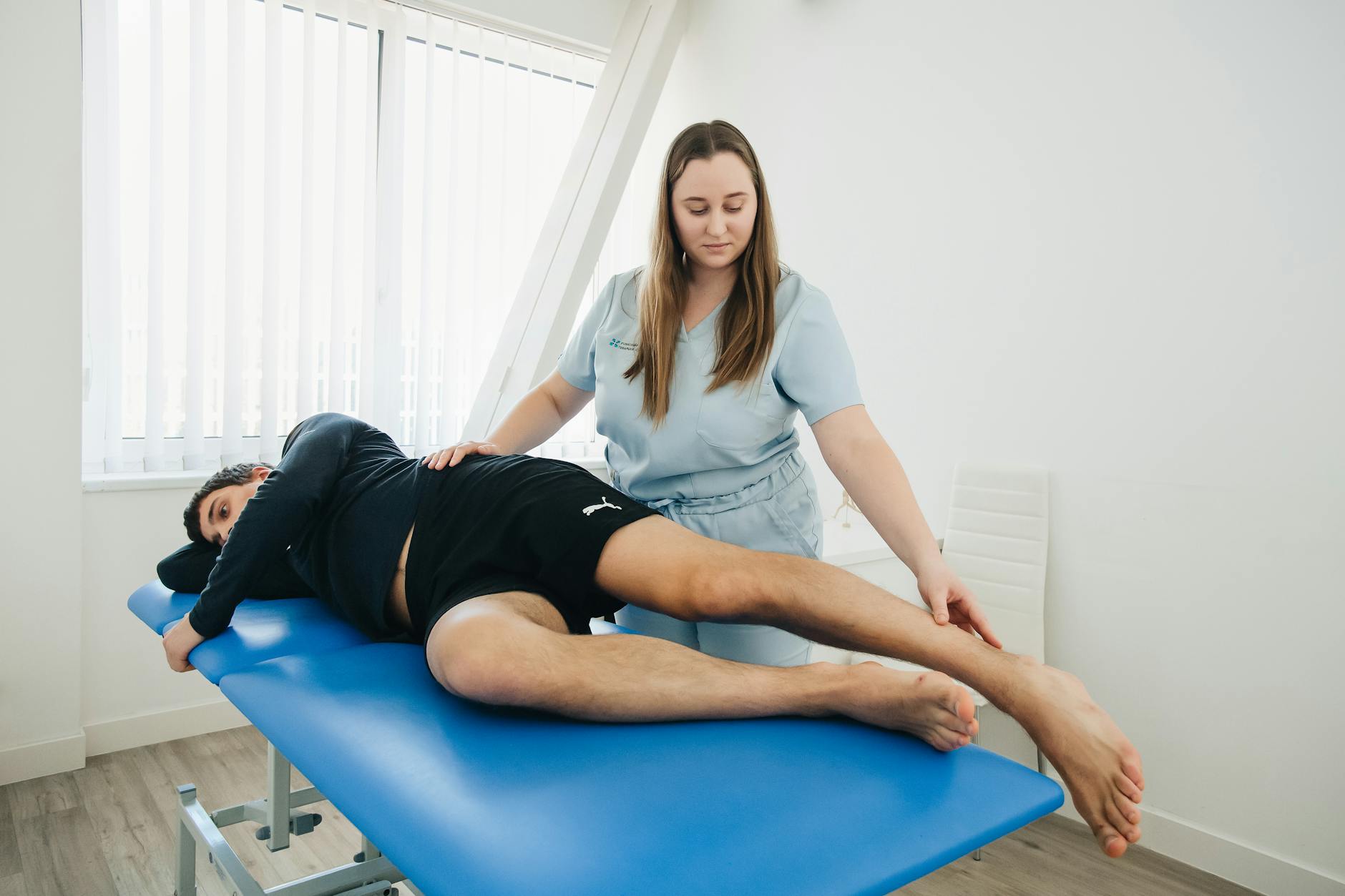
Cel czytelnika: uporządkować wiedzę i zbudować spójny plan pracy
Osoba pracująca z pacjentami neurologicznymi zwykle szuka sposobu, by z chaosu objawów, leków i technik terapeutycznych ułożyć przejrzysty, powtarzalny schemat działania. Celem jest zrozumienie, jak połączyć modulację napięcia mięśniowego farmakologicznie z terapią manualną i treningiem funkcjonalnym tak, aby każda z metod wzmacniała pozostałe, zamiast z nimi kolidować.
Nowoczesne podejście do spastyczności zakłada, że farmakoterapia, praca manualna i trening ruchowy są trzema elementami jednego procesu, a nie trzema oddzielnymi światami. Dopiero ich świadome połączenie pozwala zmienić sztywny, bolesny wzorzec w bardziej funkcjonalny ruch w realnych czynnościach dnia codziennego.
Słowa kluczowe (SEO): modulacja napięcia mięśniowego, skala Ashworth i Tardieu, toksyna botulinowa a trening, planowanie terapii po baclofenie, terapia manualna przy spastyczności, trening funkcjonalny po udarze, spastyczność a ból i przykurcze, koordynacja zespołu neurorehabilitacji, strategie rozciągania aktywnego, monitorowanie efektów leczenia spastyczności, przygotowanie pacjenta do redukcji leków
Czym dziś jest spastyczność – spojrzenie kliniczne i funkcjonalne
Spastyczność w klasycznym ujęciu neurologicznym
W klasycznym ujęciu neurologicznym spastyczność definiuje się jako prędkościowo-zależny wzrost napięcia mięśniowego z nasilonym odruchem na rozciąganie, wynikający z uszkodzenia górnego neuronu ruchowego. Oznacza to, że im szybciej rozciągamy mięsień, tym silniejszy opór stawia, często z charakterystycznym „zacięciem” i nagłym puszczeniem – tzw. objaw noża sprężynowego.
Podłoże leży w zaburzonej równowadze pomiędzy drogami zstępującymi hamującymi a pobudzającymi motoneurony w rdzeniu kręgowym. W praktyce oznacza to, że mięśnie reagują nadmiernie na bodźce rozciągające, dotykowe czy bólowe, a odruchy ścięgniste są wzmożone. Klasyczne badanie neurologiczne – ocena tonusu, odruchów, objaw Babińskiego – pozwala zlokalizować problem, ale mówi niewiele o konsekwencjach funkcjonalnych.
W badaniu biernym spastyczność jest często opisywana za pomocą skal, jednak rzeczywista trudność terapeuty polega na przełożeniu tych danych na decyzje dotyczące farmakoterapii, doboru technik manualnych oraz konstrukcji treningu funkcjonalnego.
Spastyczność jako problem ruchowy i funkcjonalny
Z perspektywy neurorehabilitacji spastyczność przestaje być tylko „wysokim napięciem”. Staje się problemem ruchu i funkcji – wpływa na chód, chwyt, transfery, pielęgnację, a także na ból, zmęczenie i jakość życia pacjenta. Ten sam poziom napięcia mierzony skalą może mieć zupełnie inne znaczenie u pacjenta leżącego i u osoby chodzącej z asekuracją.
Kluczowe pytania brzmią:
- Czy spastyczność utrudnia daną czynność (np. zakładanie buta, chwytanie kubka, zmianę pozycji)?
- Czy spastyczność pomaga kompensować niedowład (np. „usztywnia” kończynę dolną, pozwalając na podporowy chód)?
- Jak spastyczność wpływa na bóle, zmęczenie, przykurcze i ryzyko odleżyn?
Nowoczesne podejście traktuje spastyczność jako zaburzony, ale wciąż używalny „materiał”. Zamiast maksymalnie ją znosić, celem jest modulacja napięcia mięśniowego, tak aby odzyskać możliwie największą kontrolę aktywną i poprawić jakość ruchu w typowych aktywnościach dnia codziennego.
Spastyczność, dystonia, sztywność, przykurcz – różnice praktyczne
Przy badaniu neurologicznym i planowaniu terapii istotne jest rozróżnienie kilku zjawisk, które łatwo wrzucić do jednego worka „napięcie”. W praktyce klinicznej pomaga kilka prostych kryteriów:
- Spastyczność – prędkościowo-zależny opór przy rozciąganiu; typowy objaw noża sprężynowego; często asymetryczna, częściej dystalna (np. zgięcie nadgarstka, palców).
- Sztywność (rigidity) – opór stały, niezależny od prędkości ruchu, często w całym zakresie; typowa w parkinsonizmie; brak „zacięcia i puszczenia”.
- Dystonia – mimowolne, skręcające ruchy i utrwalone ustawienia, często zmienne w czasie, nasilające się przy próbie ruchu lub emocjach; napięcie nie musi być prędkościowo-zależne.
- Przykurcz – strukturalne skrócenie tkanek miękkich (mięśni, powięzi, torebek), ograniczające bierny zakres ruchu także przy bardzo wolnym, technicznie poprawnym rozciąganiu; utrwalony stan, zwykle wynik długotrwałej spastyczności lub unieruchomienia.
Rozróżnienie ma znaczenie praktyczne: farmakoterapia spastyczności ma ograniczony wpływ na przykurcz strukturalny, natomiast terapia manualna może zadziałać zarówno na komponentę spastyczną (odruchową), jak i tkankową, o ile proces nie jest skrajnie zaawansowany.
Spastyczność „zła” i „użyteczna” – kiedy hamować, kiedy wykorzystywać
Spastyczność bywa postrzegana jako wróg, którego trzeba zniszczyć. Tymczasem w wielu przypadkach pełni rolę awaryjnego wspomagacza stabilizacji i ruchu. U pacjenta z głębokim niedowładem czy porażeniem, wzmożone napięcie prostowników kończyny dolnej może umożliwiać:
- utrzymanie pozycji stojącej przy asekuracji,
- wykonanie kilku kroków chodu podporowego,
- stosunkowo łatwiejsze transfery (siad–stanie–siad).
Ta sama spastyczność – jeśli nadmierna, bolesna, powodująca skurcze nocne i przykurcze – stanie się przeszkodą. Spastyczność „zła” to taka, która:
- zwiększa ból i utrudnia pielęgnację, ubieranie, higienę,
- powoduje urazowe obciążenia stawów (np. stopa końsko-szpotawa, palce młoteczkowate),
- blokuje rozwój funkcji (np. ręka zaciśnięta w pięść, brak możliwości otwarcia dłoni w żadnej aktywności).
Decyzja o włączeniu lub modyfikacji farmakoterapii, zastosowaniu toksyny botulinowej czy intensyfikacji terapii manualnej powinna wynikać właśnie z równowagi między użytecznością a szkodliwością spastyczności. Częstą pułapką jest zbyt agresywne „prostowanie” pacjenta, które pozbawia go jedynej dostępnej strategii stabilizacji.
Profile spastyczności w różnych jednostkach chorobowych
W zależności od jednostki chorobowej obraz spastyczności wygląda odmiennie i wymusza inne akcenty w terapii:
- Udar mózgu – często półkule mózgu, jednostronny niedowład. Typowy wzorzec: kończyna górna w zgięciu i pronacji, kończyna dolna w wyproście i stopa końsko-szpotawa. Spastyczność narasta zwykle po kilku tygodniach od incydentu. Główny cel: poprawa funkcji ręki i jakości chodu.
- Stwardnienie rozsiane (SM) – zmiany rozsiane w OUN, obraz bywa bardzo zróżnicowany. Spastyczność często dotyczy obu kończyn dolnych, współwystępuje z męczliwością, zaburzeniami czucia. Cele: redukcja bólu, poprawa chodu na dłuższych dystansach, ułatwienie pielęgnacji.
- Mózgowe porażenie dziecięce (MPD) – zaburzenie rozwojowe, spastyczność towarzyszy kształtowaniu się wzorców ruchowych. Napięcie wpływa na rozwój przykurczów i deformacji kostno-stawowych. Cele: profilaktyka przykurczów, wspieranie rozwoju motorycznego, zapewnienie możliwie największej samodzielności w wieku dorosłym.
- Uraz rdzenia kręgowego – spastyczność często pojawia się po okresie wstrząsu rdzeniowego, może być uogólniona lub odcinkowa, bywa wyzwalana przez bodźce bólowe, infekcje, pełny pęcherz. Cele: kontrola skurczów, profilaktyka urazów i odleżyn, ułatwienie transferów i pielęgnacji.
Przykład kliniczny: gdy „wyprostowanie” pacjenta szkodzi
Pacjent po udarze, kilka miesięcy od incydentu, chodził z asekuracją laski. Jego chód był sztywny, z wyprostowaną kończyną dolną po stronie niedowładnej i niewielkim zgięciem biodra. Lekarz, widząc wysokie napięcie prostowników i stopy, zdecydował o agresywnej farmakoterapii spastyczności – wysokie dawki baclofenu doustnego, a następnie toksyna botulinowa w mięśnie łydki i prostowniki kolana.
Po kilku tygodniach napięcie spadło. Skala Ashworth pokazywała niższe wartości, ale pacjent przestał samodzielnie chodzić. Brakowało mu „sztywnej nogi”, która wcześniej pełniła rolę pseudoprotezy. Bez równoległego programu wzmacniania mięśni, treningu równowagi i reedukacji chodu pacjent utracił funkcję, którą miał mimo gorszego jakościowo wzorca.
Przykład pokazuje, że redukcja spastyczności bez myślenia o funkcji może paradoksalnie obniżać poziom samodzielności. Nowoczesne podejście zakłada plan: co chcemy osiągnąć po obniżeniu napięcia i jak zabezpieczymy nową, niższą linię bazową za pomocą terapii manualnej i treningu funkcjonalnego.

Ocena spastyczności – od skali do analizy ruchu
Skale kliniczne i pomiary – jak czytać wyniki
Najczęściej stosowaną skalą jest Modified Ashworth Scale (MAS). Pozwala ona ocenić opór mięśni na bierne rozciąganie w skali 0–4 (z dodatkiem 1+). Jest prosta, szybka, dobrze znana lekarzom i fizjoterapeutom. Jej zalety to:
- łatwość zastosowania w warunkach klinicznych,
- możliwość śledzenia zmian w czasie po włączeniu leków czy toksyny botulinowej,
- „wspólny język” przy opisie stanu pacjenta w dokumentacji.
Ograniczenia MAS są jednak istotne:
- ocenia jedynie bierny opór, nie mówi nic o funkcji,
- jest wrażliwa na sposób badania (prędkość, doświadczenie badającego),
- nie rozróżnia komponenty odruchowej od strukturalnego przykurczu,
- nie daje informacji o selektywnej kontroli ruchu.
Dlatego kolejny krok to zastosowanie skali Tardieu, która lepiej oddaje prędkościowo-zależny charakter spastyczności, rozróżniając:
- R1 – kąt, przy którym pojawia się „zacięcie” przy szybkim rozciąganiu,
- R2 – pełny bierny zakres ruchu przy bardzo wolnym rozciąganiu.
Różnica R2–R1 pokazuje, jak duża jest komponenta dynamiczna (odruchowa). Duża różnica sugeruje, że znaczna część ograniczenia wynika z samej spastyczności, a nie z przykurczu. Mała różnica (R1 zbliżone do R2) wskazuje na utrwalone skrócenie tkanek – tu farmakoterapia ma ograniczoną skuteczność, a większe znaczenie zyskuje terapia manualna i ewentualna korekcja ortopedyczna.
Różnice między oceną w leżeniu a w aktywności
Ocena w leżeniu jest koniecznym punktem wyjścia, ale często pokazuje tylko część obrazu. U wielu pacjentów „spastyczność wychodzi” dopiero przy:
- pionizacji,
- chodzie,
- przenoszeniu ciężaru ciała,
- aktywności ręki nad głową czy w podporze.
W leżeniu mięsień może stawiać niewielki opór, a przy szybszym chodzie stopa zaczyna „uciekać” w zgięcie podeszwowe i inwersję. Dlatego ocena spastyczności powinna zawsze obejmować obserwację funkcjonalną:
- chód (zwrócenie uwagi na fazę podporu, przeniesienia, reakcję stopy na kontakt z podłożem),
- siad (stabilizacja tułowia, ustawienie stawów biodrowych i kolanowych),
- zmianę pozycji (łóżko–wózek, wózek–fotel, siad–stanie),
- czynności manualne: chwyt, manipulację, podporowe użycie ręki (np. przy wstawaniu).
Analiza ruchu i ocena funkcjonalna jako klucz do planowania terapii
Skale napięcia mówią, jak bardzo sztywny jest mięsień. Analiza ruchu pokazuje, jak pacjent radzi sobie z zadaniem. To dwa różne światy. Dopiero ich połączenie pozwala zdecydować, czy spastyczność głównie blokuje, czy jeszcze pomaga.
Prosty przykład porównawczy:
- Pacjent A – wysoka MAS w zginaczach palców ręki, ale potrafi złapać kubek, oprzeć się na dłoni, korzysta z ręki podporowo. Spastyczność jest „głośna” w badaniu, lecz częściowo użyteczna funkcjonalnie.
- Pacjent B – podobny wynik MAS, ale ręka stale zaciśnięta, skóra w zagłębieniach dłoni drażniona, trudności z higieną, brak jakiegokolwiek użycia funkcjonalnego. Tu taka sama liczba w skali oznacza realną barierę.
Analiza funkcjonalna powinna obejmować:
- Jakość strategii kompensacyjnych – czy pacjent „blokuje” stawy, czy ma choć minimalne sterowanie ekscentryczne?
- Dostępność pozycji – które ustawienia ciała prowokują wzrost spastyczności (np. szybka pionizacja, chwyt z szybką supinacją), a które ją wyciszają.
- Zmęczenie – czy z każdym powtórzeniem pojawia się narastające „szarpanie” ruchu, czy przeciwnie, mięsień „odpuszcza” po kilku ruchach?
- Wpływ bólu i emocji – wzrost spastyczności przy dyskomforcie, stresie, hałasie często jest silniejszy niż przy samym rozciąganiu.
Na tej podstawie można zdecydować, gdzie głównym celem będzie redukcja napięcia (np. dla poprawy higieny i snu), a gdzie raczej uczenie pacjenta korzystania z istniejącego napięcia dla stabilizacji lub przenoszenia ciężaru.
Technologie wspierające ocenę – kiedy naprawdę pomagają
W praktyce stosowane są różne narzędzia od prostych po bardzo zaawansowane. Ich użyteczność wyraźnie różni się w zależności od ośrodka i pytania klinicznego.
- Prosta analiza wideo – nagrania chodu, siadania, transferów z użyciem telefonu czy tabletów. Plusy: tania, łatwa, pozwala porównać ruch „przed” i „po” leczeniu farmakologicznym lub blokadach. Minusy: subiektywna interpretacja, brak twardych danych liczbowych.
- Systemy do analizy chodu 2D/3D – kamery, platformy dynamometryczne, czasem EMG powierzchniowe. Dają szczegółowe informacje o kątach stawowych, czasie faz chodu, aktywności mięśni. Sprawdzają się przy planowaniu większych interwencji (np. operacje ortopedyczne, wielopoziomowe ostrzykiwanie toksyną). Wadą jest koszt, ograniczona dostępność i czasochłonność badania.
- Akcelerometry, czujniki inercyjne – mobilne czujniki przyczepiane do segmentów ciała. Pozwalają ocenić ruch w warunkach zbliżonych do naturalnych (np. przez kilka godzin w ciągu dnia). Dobre narzędzie do weryfikacji, jak pacjent realnie chodzi w domu, a nie tylko na krótkim odcinku w gabinecie.
W ośrodkach o mniejszych możliwościach sprzętowych kluczowe pozostaje dobre kliniczne „oko”: umiejętność powiązania wzorca ruchu z konkretnymi grupami mięśniowymi i ustawieniami stawów. Technologia jest wtedy dodatkiem, nie zastępstwem oceny manualnej.
Farmakoterapia spastyczności – możliwości, ograniczenia i konsekwencje dla fizjoterapii
Leki doustne zmniejszające napięcie – kto korzysta najbardziej
Najczęściej stosowane leki ogólnoustrojowe to m.in. baklofen, tizanidyna, benzodiazepiny, dantrolen. Każdy z nich działa inaczej, a ich efekt funkcjonalny bywa bardzo różny w zależności od profilu pacjenta.
- Baklofen – agonista receptorów GABAB w rdzeniu kręgowym, zmniejsza pobudliwość łuku odruchowego. Zwykle preferowany przy uogólnionej spastyczności (np. SM, uraz rdzenia). Zaletą jest wyraźna redukcja skurczów nocnych i bólu. Wadą: senność, osłabienie siły, możliwe pogorszenie równowagi.
- Tizanidyna – działa presynaptycznie na interneurony, zmniejszając napięcie mięśni. Bywa użyteczna, gdy potrzebna jest umiarkowana redukcja spastyczności z mniejszym ryzykiem globalnego „wyłączenia” pacjenta, choć sedacja i hipotonia ortostatyczna nadal są częste.
- Benzodiazepiny – mocny efekt przeciwskurczowy i przeciwlękowy, ale znacząco upośledzają czujność. Lepsze w krótkotrwałym użyciu (np. w okresach zaostrzenia skurczów, po zabiegach), rzadziej jako stała terapia u osób mobilnych.
- Dantrolen – hamuje uwalnianie wapnia w mięśniach, działając bezpośrednio na włókno mięśniowe. Może redukować siłę potrzebną w ruchu funkcjonalnym, a przy dłuższym stosowaniu wymaga monitorowania wątroby.
Jeśli porównać dwie grupy:
- osoby leżące lub w dużej mierze zależne – często odnoszą większą korzyść z ogólnej redukcji napięcia (mniejszy ból, mniej skurczów, łatwiejsza pielęgnacja),
- osoby chodzące z kompensacjami – tu agresywne dawki mogą zabrać jedyną dostępną stabilizację. U tej grupy lepiej sprawdzają się mniejsze dawki, stopniowo modyfikowane równolegle z intensywną fizjoterapią.
Toksyczna botulinowa – precyzyjna ingerencja czy „wyłączenie” mięśnia
Toksyna botulinowa typu A jest narzędziem celowanego osłabiania aktywności wybranych mięśni. Różnica w stosunku do leków doustnych jest zasadnicza: działanie jest miejscowe, dawka ograniczona, a efekt czasowy (średnio 3–4 miesiące).
Najczęstsze wskazania funkcjonalne:
- ręka po udarze – nadmierne zgięcie nadgarstka, palców, kciuka utrudniające otwarcie dłoni, higienę, zakładanie ortez,
- stopa końsko-szpotawa – utrwalony wzorzec, który uniemożliwia kontakt pięty z podłożem i powoduje urazy skóry,
- spastyczność przywodzicieli biodra – problemy z higieną krocza, siadaniem okrakiem, transferami z rozstawieniem nóg,
- bolesne skurcze segmentowe (np. zginacze łokcia) ograniczające ubieranie, mycie, pozycjonowanie.
Ta sama toksyna u dwóch pacjentów może dać zupełnie inne skutki:
- U pacjenta, który nie używa kończyny funkcjonalnie, lecz ma duży ból i problemy z pielęgnacją, ostrzyknięcie kilku mięśni wyraźnie poprawi komfort i ułatwi codzienność.
- U osoby, która weszła w kompensacyjny, ale stabilny wzorzec (np. „sztywna” noga do chodu podporowego), zbyt szerokie ostrzyknięcie może doprowadzić do utraty chodu, jeśli nie towarzyszy temu plan intensywnej przebudowy wzorca.
Przy planowaniu ostrzyknięcia warto odpowiedzieć na kilka pytań:
- Jakie zadania funkcjonalne chcemy poprawić w pierwszej kolejności (np. higiena, chód, ubieranie)?
- Które mięśnie są rzeczywiście nadaktywne odruchowo, a które tylko skrócone strukturalnie?
- Jaki jest plan terapii manualnej i treningu funkcjonalnego na kolejne tygodnie po zabiegu?
Baklofen podpajęczynówkowy – rozwiązanie dla ciężkiej, uogólnionej spastyczności
U pacjentów z bardzo nasilonym, uogólnionym wzmożeniem napięcia (często po urazach rdzenia, w ciężkich postaciach MPD, SM) rozważa się pompę baklofenową. Lek podawany jest bezpośrednio do kanału kręgowego, co pozwala na mniejsze dawki ogólne przy silniejszym efekcie lokalnym.
Porównując ten sposób podania z baklofenem doustnym, różnice są wyraźne:
- Skuteczność przeciwskurczowa – wyższa w podaniu podpajęczynówkowym, szczególnie przy spastyczności tułowia i kończyn dolnych.
- Działania niepożądane ogólnoustrojowe – zwykle mniejsze, choć w przypadku nadmiernej dawki możliwy jest silny spadek napięcia posturalnego.
- Inwazyjność – wymiana, serwis pompy, ryzyko powikłań zabiegowych, konieczność monitorowania.
Największą korzyść odnoszą osoby:
- z bardzo bolesną, utrudniającą pielęgnację spastycznością,
- u których cele funkcjonalne dotyczą głównie komfortu, pielęgnacji, pozycji siedzącej i leżącej, a nie samodzielnego chodu bez pomocy.
Dla fizjoterapeuty oznacza to inny akcent pracy: mniej walki z oporem w biernych ruchach, więcej miejsca na pozycjonowanie, profilaktykę przykurczów strukturalnych i automatyzację bezpiecznych transferów.
Konsekwencje farmakoterapii dla planu fizjoterapii
Zmiana napięcia mięśniowego to zmiana całej „mechaniki” pacjenta. Fizjoterapeuta musi szybko przestawić strategię, inaczej pacjent „zgubi” to, co zyskał farmakologicznie.
Po włączeniu lub zwiększeniu dawek leków przeciwspastycznych zwykle pojawia się kilka zjawisk:
- Spadek oporu w biernym ruchu – łatwiej pracować manualnie w większym zakresie, możliwe jest wprowadzenie bardziej złożonych mobilizacji i treningu ekscentrycznego.
- Poczucie „miękkości” i niepewności – pacjent, który latami „polegał” na sztywnych nogach, nagle traci ten „gips”. Często zgłasza większy lęk przed upadkiem mimo obiektywnie lepszych warunków do ruchu.
- Zmęczenie mięśni – dawniej większość ruchu „robił” odruch, teraz więcej pracy przypada mięśniom działającym wolniej, selektywnie. Trening siły i wytrzymałości staje się konieczny.
Dlatego farmakoterapia powinna iść równolegle z:
- treningiem kontroli posturalnej (w siadzie, staniu, klęku, podporach),
- wzmacnianiem mięśni antagonistycznych do wcześniej spastycznych (np. prostowników kolana przy redukcji spastyczności zginaczy, i odwrotnie),
- reedukacją czucia i schematu ciała – pacjent musi „nauczyć się” nowej odpowiedzi proprioceptywnej przy ruchu w większym zakresie,
- stopniową ekspozycją na zadania trudniejsze (np. chód po różnych nawierzchniach) po ostrzyknięciu toksyną, zanim minie okres największego efektu.
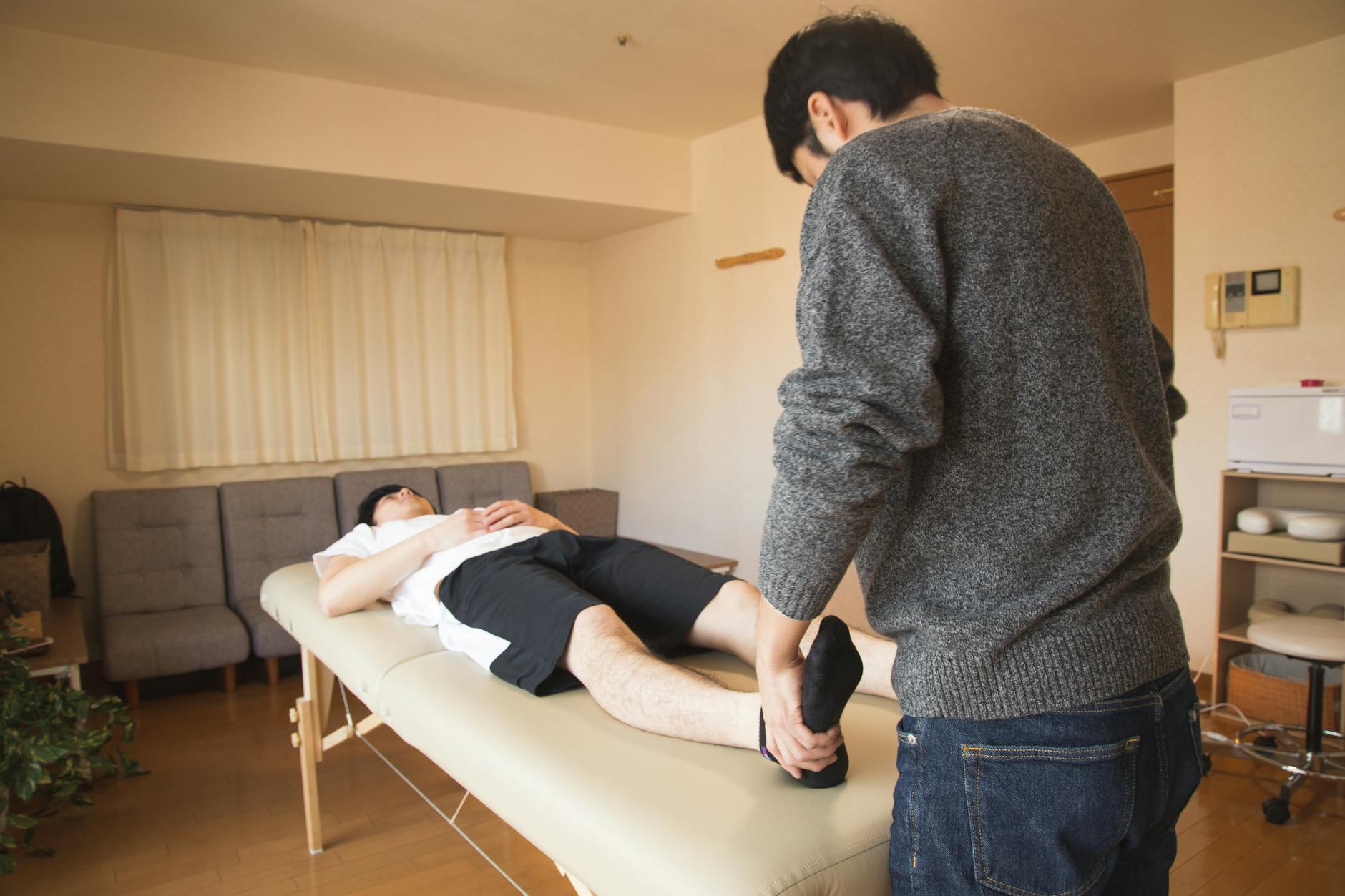
Terapia manualna przy spastyczności – od „rozluźniania” do pracy na kontroli ruchu
Techniki o działaniu głównie tonolitycznym
Wiele technik manualnych ma przede wszystkim działanie objawowe – obniża napięcie na czas sesji i krótko po niej. Nadal są potrzebne, ale ich rola różni się w zależności od celu:
- Delikatne, długotrwałe rozciąganie – powolne prowadzenie segmentu z kontrolą oddechu pacjenta. Dobre przed ćwiczeniami funkcjonalnymi, by „otworzyć okno” z mniejszym napięciem.
- Trakcje i mobilizacje stawowe o małej amplitudzie – szczególnie przy stawach bolesnych, przeciążonych przez długotrwałą spastyczność. Dają ulgę bólową i poprawiają czucie stawu.
- Miękkie techniki powięziowe – praca na pasmach powięzi, które przez lata dostosowywały się do patologicznego wzorca. Pomagają zmniejszyć „ciągnięcie” tkanek przy próbie zmiany ustawienia kończyny.
U pacjenta, który ma głównie cele pielęgnacyjne (pozycjonowanie, brak bólu w spoczynku), te techniki mogą stanowić znaczną część terapii. Natomiast u osoby, która chce poprawić chód czy funkcję ręki, traktuje się je raczej jako wstęp do bardziej aktywnej pracy.
Praca na przykurczu vs. praca na komponencie odruchowej
Terapia manualna przy spastyczności zawsze balansuje między dwoma obszarami:
- przykurcz strukturalny – wymaga czasu, systematyczności, często współpracy z ortezoterapią,
- nadmierna odpowiedź odruchowa – reaguje na tempo ruchu, kierunek, bodźce dotykowe.
Przy porównaniu dwóch pacjentów z podobnie zgiętym łokciem:
- u pierwszego łokieć otwiera się prawie do pełnego wyprostu przy bardzo wolnym, dobrze prowadzonym ruchu – dominuje komponenta odruchowa,
Strategie pracy przy dominacji komponenty odruchowej
Jeśli dominuje odruchowa część spastyczności, kluczowe stają się: tempo, kierunek, sposób prowadzenia ruchu oraz kontrola bodźców czuciowych. Te same stopnie ruchu, wykonane w różny sposób, mogą dać skrajnie różną odpowiedź napięciową.
- Zwolnienie tempa i przewidywalność – ruch prowadzony bardzo wolno, w zaplanowanym kierunku, z wyprzedzającą informacją słowną. Nagłe „szarpnięcia” czy korekty toru ruchu potrafią natychmiast „włączyć” wzmożony odruch.
- Zmiana kolejności segmentów – najpierw ustawienie bliższego segmentu (np. łopatki, miednicy), dopiero potem dalszego (łokcia, kolana). W wielu przypadkach odpowiednie ustawienie proksymalne już częściowo wycisza nadreaktywność dystalną.
- Redukcja bodźców noxalnych – zimno, ból, ucisk, drażniący dotyk skóry nasila odpowiedź odruchową. Ciepłe środowisko, wygodna pozycja, miękkie podparcia i łagodny kontakt dłonią często obniżają „próg wyzwolenia” spastyki.
U osoby, która reaguje gwałtownym skurczem na szybkie zgięcie stawu skokowego, ruch w tym samym kierunku, wykonany powoli, przy wcześniejszym rozluźnieniu zginaczy biodra i kolana, bywa możliwy w znacznie większym zakresie. Różnica nie wynika z „rozciągnięcia” tkanek, ale z innej odpowiedzi układu nerwowego.
Strategie pracy przy dominacji przykurczu strukturalnego
Przy utrwalonym skróceniu tkanek (mięśni, powięzi, torebek stawowych) priorytetem staje się dawka bodźca w czasie – nie siła jednorazowego rozciągnięcia. Manualnie można wprowadzić tkanki w nowy zakres, lecz utrwalenie wymaga odpowiedniej „higieny pozycji” i ortezoterapii.
- Długotrwałe pozycjonowanie – zamiast kilku minut intensywnego rozciągania lepsze są godziny w umiarkowanie skorygowanej pozycji (ortezy nocne, szyny dynamiczne, kliny pod kolana, siedziska z regulacją kątów).
- Stopniowe przesuwanie bariery końcowej – terapeuta co kilka sesji zmienia ustawienie ortezy o kilka stopni, a w trakcie terapii manualnej szanuje granicę bólu, unikając mikro-urazów, które prowokują większą spastykę.
- Praca na tkankach okołostawowych – mobilizacje torebki stawowej, powięzi i mięśni synergistycznych. Utrwalony przykurcz zginaczy łokcia rzadko dotyczy tylko bicepsa – stwardniałe pasma przedramienia, ograniczona ślizgowość nerwu pośrodkowego czy łokciowego także bywają ograniczeniem.
Różnica w strategii jest wyraźna: przy komponencie odruchowej celem jest „uspokojenie” odpowiedzi i stworzenie okna do ruchu, przy przykurczu – dostarczenie długotrwałego, nieprzeciążającego bodźca przebudowującego tkankę.
Łączenie terapii manualnej z ruchem aktywnym „od razu”
Skuteczność manualnej pracy przy spastyczności rośnie, gdy bezpośrednio po niej następuje zadanie ruchowe, które wykorzystuje nowy zakres. „Rozluźniony” mięsień bez nowego nawyku szybko wraca do poprzedniego wzorca.
Przykładowe sekwencje:
- rozluźnienie zginaczy palców ręki + mobilizacje nadgarstka → od razu chwyt cylindryczny dużego przedmiotu, podparcie na otwartej dłoni, ćwiczenia przenoszenia ciężaru na rękę,
- mobilizacje stawu skokowego i powięzi łydki → następnie stanie przy poręczy z naciskiem na piętę, później chód po równym podłożu z koncentracją na fazie kontaktu pięty,
- praca na zgięciowym przykurczu biodra → potem ćwiczenia wydłużania kończyny w podporze przodem do ściany, kroki w tył, przejścia z siadu do stania z wyraźnym „wyprostowaniem się” w biodrze.
Różnica między „klasycznym” podejściem (sesja manualna, potem bierne ćwiczenia) a zintegrowanym jest taka, że w tym drugim mięsień od razu zostaje włączony w zadanie celowe. Ośrodkowy układ nerwowy dostaje nowy „scenariusz”: inna długość mięśnia + nowe zadanie = inny zapis ruchu.
Rola kontroli proksymalnej w manualnym przygotowaniu do treningu
Wzmożone napięcie często „ucieka” do segmentów bliższych: ramienia, łopatki, miednicy. Terapia skupiona wyłącznie na dłoni czy stopie bez pracy nad tułowiem przypomina prostowanie gałęzi przy skręconym pniu.
Manualnie można:
- ustabilizować segment bliższy (np. miednicę w ustawieniu pośrednim) i pracować na wolniejszym, kontrolowanym ruchu kończyny dolnej,
- poprawić ślizg i ustawienie łopatki, zanim zacznie się pracę nad prostowaniem łokcia i otwieraniem dłoni,
- wyciszyć napięcie mięśni przykręgosłupowych u osób z silną spastyką tułowia, zanim wprowadzi się trening równoważny w siadzie.
W praktyce widać wyraźną różnicę: pacjent po rozluźnieniu i ustawieniu miednicy oraz dolnego odcinka kręgosłupa znacznie lepiej toleruje rozciąganie zginaczy biodra, a zakres ruchu uzyskany w trakcie sesji manualnej ma większą szansę utrzymać się, jeśli zaraz potem nastąpi aktywne „zakotwiczenie” w nowej pozycji.
Dotyk tonizujący vs. dotyk wyciszający
Osoby ze spastycznością reagują na dotyk silniej niż pacjenci ortopedyczni. Sposób kontaktu dłoni terapeuty może działać pobudzająco lub uspokajająco.
- Dotyk wyciszający – szeroka powierzchnia dłoni, stały nacisk, brak szybkich zmian kierunku. Sprawdza się przy rozpoczęciu sesji, na odcinkach o silnej reaktywności (przednia część uda, łydka, zginacze palców).
- Dotyk bardziej tonizujący/aktywujący – nieco szybszy, z wyraźniejszym kierunkowym prowadzeniem, przydatny gdy chcemy „obudzić” antagonistów spastycznego mięśnia lub wprowadzić pacjenta w mobilizację globalną (np. rotacje tułowia w leżaniu).
Dobór rodzaju dotyku zależy od aktualnego celu: przed ćwiczeniem równoważnym zwykle korzysta się częściej z dotyku wyciszającego, by obniżyć nadmierną reakcję mięśniową; przed zadaniami siłowymi antagonistów – z dotyku bardziej tonizującego, który pomaga w rekrutacji włókien mięśniowych.
Manualne przygotowanie do ortezoterapii i zabiegów inwazyjnych
Terapia manualna może pełnić rolę „testera” i „przygotowania” przed włączeniem ortez lub zabiegów takich jak toksyna botulinowa czy wydłużanie ścięgien.
- Symulacja działania ortezy – terapeuta ustawia kończynę w pozycji zbliżonej do tej, jaką zapewni planowana orteza (np. lekko wyprostowany łokieć, stopa w neutralu) i obserwuje, jak zmienia się funkcja oraz napięcie w trakcie ruchu. To pomaga zdecydować, czy orteza ma głównie stabilizować, czy również rozciągać.
- Ocena reakcji na tymczasowe „wyłączenie” mięśnia – jeśli przy manualnym wyciszeniu danego mięśnia (np. zginacza biodra) pacjent znacząco traci zdolność do chodu, ostrzyknięcie toksyną w tym obszarze może być ryzykowne bez intensywnego, równoległego treningu antagonisty.
- Przygotowanie do zabiegu chirurgicznego – poprawa elastyczności tkanek okołostawowych i wstępne „nauczenie” pacjenta nowych ustawień kończyny ułatwiają późniejszą rehabilitację po wydłużeniach chirurgicznych.
Porównując dwa scenariusze – w jednym orteza czy toksyna włączana jest „w ciemno”, w drugim poprzedzona jest manualną symulacją – w tym drugim ryzyko nietrafionego doboru mięśni lub ustawień jest wyraźnie mniejsze.
Trening funkcjonalny jako trzeci filar – od kompensacji do bardziej ekonomicznego wzorca
Trening funkcjonalny a klasyczne ćwiczenia „na siłowni rehabilitacyjnej”
Ćwiczenia izolowane (zginanie, prostowanie w pojedynczym stawie, praca w bramie wyciągowej) mają swoją rolę, ale u pacjentów ze spastycznością szybko ujawniają się ich ograniczenia. Napięcie patologiczne pojawia się głównie w zadaniach całego ciała – chód, wstawanie, transfery, podparcie na rękach, więc właśnie tam trzeba przenosić środek ciężkości treningu.
Porównując dwa podejścia:
- Trening izolowany – poprawia siłę danego mięśnia w kontrolowanych warunkach, łatwiej dozować obciążenie, mniejsze ryzyko upadku. Nie zawsze przenosi się bezpośrednio na funkcję (np. silny prostownik kolana w leżeniu nie musi gwarantować lepszego chodu).
- Trening zadaniowy – od początku angażuje kilka segmentów, konieczność kontroli posturalnej i adaptacji napięcia do celu (wstanie, obrót, krok). Trudniej go „uporządkować”, ale ostatecznie decyduje o samodzielności.
Optymalny plan łączy oba: izolowaną pracę tam, gdzie trzeba „dostarczyć siły” lub zbudować selektywność, oraz zadania funkcjonalne, aby nauczyć układ nerwowy używać tej siły w realnych sytuacjach.
Planowanie treningu w „oknie” po toksynie lub modyfikacji leków
Zmiana farmakoterapii tworzy czasowe „okno” – pacjent ma mniej spastyki, ale też często mniejszą stabilizację kompensacyjną. To okres, w którym intensywny trening funkcjonalny decyduje, czy organizm zbuduje nowy, lepszy wzorzec, czy wróci do poprzedniego.
Można wyróżnić kilka faz:
- Faza adaptacji (pierwsze dni–tydzień) – większe poczucie niestabilności, niepewność, większe zmęczenie. Tu przeważają ćwiczenia w pozycjach niskich (leżenie, siad), z dużą ilością informacji zwrotnej i asekuracji.
- Faza budowania nowych wzorców (kolejne tygodnie) – nacisk na chód, transfery, użyteczne ruchy ręki. Terapeuta stopniowo ogranicza pomoc, ale konsekwentnie wymaga wykorzystania nowego zakresu ruchu (np. pełniejszego wyprostu kolana przy staniu).
- Faza utrwalania – wdrażanie elementów treningu w środowisku domowym i społecznym (schody, podłoża o różnej twardości, czynności dnia codziennego), by wzorzec nie był „kliniczny”, ale życiowy.
Bez takiego planu pacjent często wraca po kilku miesiącach z komentarzem: „Na chwilę było lepiej, ale wszystko wróciło”. Problemem nie jest sama toksyna czy lek, lecz brak intensywnego wykorzystania okna możliwości.
Trening antagonistów i „wyrównywanie sił”
Spastyczny mięsień rzadko jest naprawdę silny – zwykle jest nadaktywny i skrócony, natomiast jego antagonista jest osłabiony i „zastraszony”. Trening funkcjonalny bez świadomego wzmacniania antagonistów sprzyja utrwalaniu nierównowagi.
- Przy spastyczności zginaczy palców – ćwiczenia chwytu otwartego, odwodzenia kciuka, podparcia na dłoni, pracy nad prostownikami nadgarstka.
- Przy przewadze zginaczy biodra i kolana – kładzie się nacisk na trening prostowników biodra (mosty, wstania z krzesła z kontrolą wyprostu), prostowników kolana i mięśni pośladkowych.
- Przy dominacji zginaczy łokcia – aktywacja tricepsa w podporach, wyprostach z oporem, ćwiczenia w zamkniętych łańcuchach (podparcie na dłoni, przesuwanie ciężaru ciała).
Różnica między „ogólnym wzmacnianiem” a celowanym treningiem antagonistów jest taka, że w tym drugim ćwiczenia dobiera się tak, by przy każdym zadaniu spastyczny mięsień musiał choć trochę wydłużyć się, a jego przeciwnik wykonywał pracę w funkcjonalnym kierunku.
Trening równowagi: od pozycji bezpiecznych do wymagających
Spastyczność często pełni funkcję „gipsu posturalnego” – usztywnia kończyny, dzięki czemu pacjent stoi lub chodzi mimo słabej kontroli tułowia. Gdy napięcie się obniża, równowaga musi zostać „dorobiona” innymi strategiami.
Stopniowanie bodźca równoważnego:
- Pozycje niskie – siad na stabilnym podłożu, podpory przodem i bokiem, klęk podparty. Celem jest odzyskanie kontroli tułowia bez dużego ryzyka upadku.
- Pozycje pośrednie – klęk jednonogi, wysoki klęk, stanie przy podporze. Tu zaczyna się praca nad różnicowaniem napięcia między stroną podporową a swobodną.
- Pozycje wysokie i zadania dynamiczne – stanie bez podpory, krok w przód/bok/tył, chód po różnych nawierzchniach, reagowanie na lekkie pchnięcia.
Najczęściej zadawane pytania (FAQ)
Czym różni się spastyczność od dystonii, sztywności i przykurczu w praktyce?
Spastyczność to prędkościowo-zależny wzrost napięcia – im szybciej rozciągasz mięsień, tym większy opór czujesz, często z „zacięciem i puszczeniem” (objaw noża sprężynowego). Typowo dotyczy bardziej dystalnych odcinków, np. nadgarstka czy stopy.
Sztywność (rigidity) daje stały opór w całym zakresie ruchu, niezależny od prędkości, charakterystyczny np. dla parkinsonizmu. Dystonia to raczej skręcające, mimowolne ruchy i utrwalone ustawienia, nasilające się przy próbie ruchu czy emocjach. Przykurcz to już strukturalne skrócenie tkanek (mięśni, powięzi, torebek stawowych) – ogranicza bierny zakres ruchu nawet przy bardzo wolnym, poprawnym rozciąganiu.
W uproszczeniu: leki i toksyna botulinowa działają głównie na komponentę spastyczną (odruchową), a przykurcz wymaga pracy na tkankach (terapia manualna, rozciąganie, ortezy, czasem operacja). Sztywność i dystonia reagują inaczej na leczenie niż typowa spastyczność, dlatego precyzyjna diagnoza ma znaczenie dla planu terapii.
Kiedy spastyczność „pomaga”, a kiedy trzeba ją zdecydowanie hamować?
Spastyczność bywa użyteczna, gdy częściowo „podmienia” siłę mięśniową. U pacjentów z głębokim niedowładem kończyny dolnej wzmożone napięcie prostowników może ułatwiać stanie z asekuracją, wykonanie kilku kroków podporowych czy transfer z łóżka na wózek.
Za „złą” spastyczność uznaje się taką, która powoduje ból, nocne skurcze, utrudnia ubieranie, higienę i zmianę pozycji, prowadzi do przykurczów, deformacji stóp lub palców, blokuje otwarcie dłoni i rozwój funkcji. Wtedy celem jest wyraźna modulacja napięcia: farmakoterapia, toksyna botulinowa, intensywna terapia manualna i trening ruchowy ukierunkowany na odzyskanie kontroli aktywnej.
Kluczowe pytanie w praktyce brzmi: czy redukując spastyczność, nie odbieramy pacjentowi jedynej dostępnej strategii stabilizacji? Jeśli po „wyprostowaniu” pacjent przestaje chodzić lub stać, leczenie jest zbyt agresywne i wymaga korekty.
Jak połączyć toksynę botulinową, baclofen i fizjoterapię przy spastyczności?
Toksyna botulinowa działa miejscowo na wybrane mięśnie, baclofen (doustny lub dokanałowy) – ogólnoustrojowo. Toksyna daje szansę na „okno terapeutyczne” w konkretnym wzorcu (np. zgięta ręka po udarze), natomiast baclofen obniża napięcie szerzej, co bywa korzystne przy rozlanej spastyczności, ale może osłabić funkcjonalne napięcie posturalne.
Fizjoterapia powinna być zaplanowana w czasie: po podaniu toksyny warto zwiększyć intensywność terapii manualnej i treningu funkcjonalnego właśnie wtedy, gdy mięsień jest częściowo „uwolniony”. Po modyfikacji dawki baclofenu należy na nowo ocenić chód, transfery, możliwości podporu i dostosować ćwiczenia – często trzeba przejściowo skupić się na kontroli tułowia i stabilizacji.
Praktycznie: leki i toksyna przygotowują „grunt”, ale nie budują funkcji. To zadanie treningu ruchowego. Im lepiej fizjoterapeuta rozumie profil działania farmakoterapii, tym precyzyjniej dobierze momenty rozciągania, aktywacji i nauki nowych zadań funkcjonalnych.
Jak używać skali Ashworth i Tardieu przy planowaniu terapii spastyczności?
Skala Ashworth (i zmodyfikowana Ashworth) mierzy ogólny opór przy biernym rozciąganiu – jest prosta, ale słabo odróżnia komponentę odruchową od przykurczu strukturalnego. Dobrze sprawdza się jako szybki, porównawczy zapis zmian napięcia w czasie, np. przed i po włączeniu leku.
Skala Tardieu uwzględnia różne prędkości rozciągania i pozwala odróżnić „czystą” spastyczność od sztywności tkanek. Informuje nie tylko „ile jest napięcia”, ale też przy jakiej prędkości i w jakim kącie pojawia się „zacięcie”. Dzięki temu ułatwia np. decyzję, czy dominująca jest komponenta odruchowa (korzystna odpowiedź na leki i toksynę), czy raczej utrwalony przykurcz (priorytet dla terapii manualnej, ortez, ewentualnie chirurgii).
Użyteczne podejście łączy ocenę w skalach z analizą funkcji: ten sam wynik Ashworth u pacjenta leżącego i u chodzącego może mieć zupełnie inne znaczenie kliniczne. Zapisy ze skal są więc punktem wyjścia, a nie jedyną podstawą decyzji terapeutycznych.
Jak planować terapię manualną i rozciąganie u pacjentów ze spastycznością?
Terapia manualna przy spastyczności nie polega wyłącznie na „mocnym rozciąganiu”. Zwykle łączy wolne, kontrolowane rozciąganie z pracą na tkanekach miękkich, torowaniem ruchu i przygotowaniem do zadania funkcjonalnego. Zbyt szybkie, agresywne techniki mogą nasilać odruch spastyczny, zamiast go wygaszać.
Sprawdza się model: najpierw modulacja napięcia (delikatna praca manualna, pozycjonowanie, powolne rozciąganie aktywne/pasywne), następnie wprowadzenie ruchu czynnego w „nowym” zakresie i dopiero później zadanie funkcjonalne, np. chwyt kubka, krok z obciążeniem. W zaawansowanych przykurczach rozciąganie krótkimi sesjami jest najczęściej niewystarczające – potrzebne są dłuższe czasy obciążenia (szyny, ortezy, pozycjonowanie).
Różnica w stosunku do klasycznego „rozciągnij i puść” jest zasadnicza: celem nie jest sam większy zakres bierny, lecz taki poziom napięcia i elastyczności tkanek, który umożliwia lepszy, bardziej ekonomiczny ruch w zadaniach dnia codziennego.
Jak trening funkcjonalny po udarze wpływa na spastyczność?
Trening funkcjonalny po udarze działa na spastyczność pośrednio – przez poprawę kontroli posturalnej, aktywnej stabilizacji i jakości ruchu. Im więcej pacjent używa kończyny w sensownych zadaniach (chwytanie, podparcie, chód), tym częściej układ nerwowy „uczy się” innych strategii niż sztywne usztywnienie.
Ćwiczenia izolowane (np. same ruchy bierne) zwykle słabo przekładają się na funkcję. Najlepsze efekty daje łączenie: po farmakologicznym obniżeniu napięcia i pracy manualnej nad zakresem ruchu wprowadza się zadania zadaniowe – wstawanie, chód po różnych podłożach, manipulację przedmiotami. Ruch jest wtedy „zakotwiczony” w realnej aktywności, a nie tylko w sali ćwiczeń.
Kluczowe Wnioski
- Spastyczność to nie tylko „wysokie napięcie”, lecz zaburzenie ruchu i funkcji – ten sam wynik w skali (Ashworth, Tardieu) może oznaczać co innego u pacjenta leżącego i u osoby chodzącej, więc decyzje terapeutyczne trzeba opierać na analizie konkretnych czynności (chód, chwyt, pielęgnacja).
- Farmakoterapia, terapia manualna i trening funkcjonalny powinny tworzyć jeden, spójny proces: leki i toksyna botulinowa modulują napięcie, praca manualna „czyści” komponentę odruchową i tkankową, a trening ruchowy uczy mózg nowych, użytecznych wzorców – żadna z tych metod nie powinna działać w oderwaniu od pozostałych.
- Kluczowe jest odróżnienie spastyczności od sztywności, dystonii i przykurczu: leki dobrze wpływają na komponentę spastyczną, natomiast w przykurczu strukturalnym dominują zadania dla terapii manualnej i odpowiedniego rozciągania; pomylenie tych zjawisk prowadzi do nieskutecznego leczenia.
- Spastyczność może być zarówno „zła”, jak i „użyteczna”: u pacjenta z ciężkim niedowładem napięcie prostowników bywa jedynym oparciem dla pozycji stojącej czy kilku kroków, natomiast u osoby z bolesnymi nocnymi skurczami i zaciśniętą dłonią to samo napięcie staje się główną barierą funkcji.
- Decyzja „kiedy hamować, a kiedy wykorzystywać spastyczność” powinna wynikać z bilansu zysków i strat: czy napięcie bardziej pomaga w kompensacji (np. podparcie kończyny dolnej w chodzie), czy częściej blokuje ruch, nasila ból, sprzyja przykurczom i odleżynom.
Źródła
- Spasticity: Diagnosis and Management. The Lancet Neurology (2013) – Przegląd definicji spastyczności, patofizjologii i podejść terapeutycznych
- Management of Adult Spasticity: A Practical Guide. Royal College of Physicians (2018) – Wytyczne kliniczne dot. leczenia spastyczności u dorosłych, farmakoterapia i rehabilitacja
- Clinical Guidelines for Stroke Management. Stroke Foundation Australia (2017) – Zalecenia postępowania po udarze, w tym ocena i leczenie spastyczności
- Guidelines for the Management of Spasticity in Children and Adolescents with Cerebral Palsy. National Institute for Health and Care Excellence (2012) – Wytyczne NICE dla MPD: toksyna botulinowa, baclofen, rehabilitacja
- The Modified Ashworth Scale and Modified Tardieu Scale: Clinical Use and Limitations. Archives of Physical Medicine and Rehabilitation (2004) – Opis skal Ashworth i Tardieu, ich zastosowanie i ograniczenia w praktyce